Le sarin est un agent neurotoxique organophosphoré dont l’histoire ne cesse de s’écrire depuis 1939. Cet article explique en détail le mécanisme d’action de l’acétylcholine et de l’acétylcholinestérase, comment le sarin bloque cette enzyme et déclenche une crise cholinergique potentiellement mortelle, et quels traitements (atropine, pralidoxime, benzodiazépines) permettent d’y répondre. Il aborde également la décontamination, le syndrome de la guerre du Golfe et le lien probable avec des expositions à de faibles doses d’organophosphorés.
1. Origine et famille chimique du sarin
On sait que le gaz sarin a été mis au point en 1939 dans les laboratoires de l’IG Farben. Sarin signifie Schrader, Ambros, Rüdiger et Van der Linde, du nom des inventeurs qui lui ont donné leurs initiales.
Il appartient à la famille des organophosphorés qui comprend des agents tels que des insecticides et aussi des agents de guerre comme les agents G : GA Tabun, GB Sarin, GD Soman, les agents V : VX et VR et les agents A, également appelés agents Novitchok (agents A-230, A-232 et A-234). Une tentative d’assassinat à l’encontre d’Alexei Navalny en 2020 a bien été perpétrée par un agent A.
2. L’acétylcholine et son rôle dans le système nerveux
L’acétylcholine (ACh) est un neuromédiateur qui joue un rôle dans le système nerveux central (mémoire, apprentissage) ainsi que dans le système nerveux périphérique (activité musculaire et fonctions végétatives).
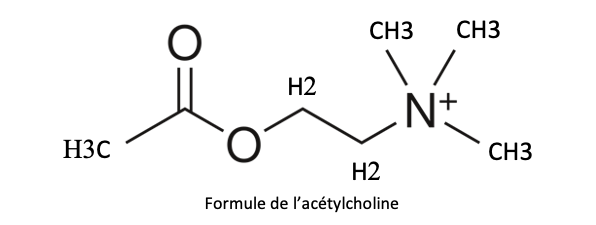
2.1. Fonctionnement de la synapse cholinergique
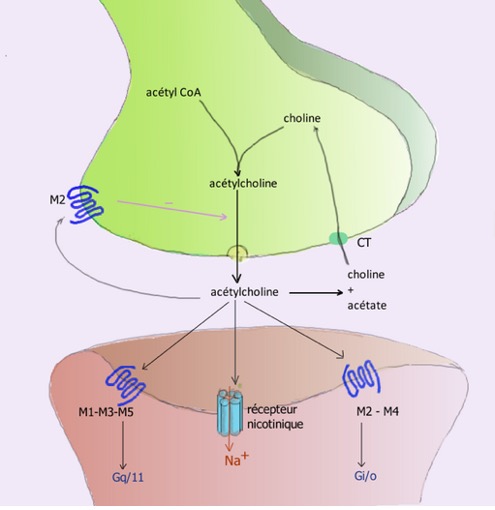
Dans un neurone, l’acétylcholine est stockée dans les vésicules de la membrane présynaptique. (Rappel : une synapse est la zone située entre la terminaison d’un neurone et soit un autre neurone, soit une cellule musculaire). Lorsqu’un potentiel d’action arrive au niveau de l’extrémité du neurone, il provoque l’ouverture de canaux à Ca++ ce qui provoque la fusion des vésicules et la libération d’ACh dans la fente synaptique. Elle parvient alors aux récepteurs postsynaptiques (c’est-à-dire de l’autre côté de la fente) et provoque une modification de la perméabilité ionique membranaire et la contraction musculaire si c’est une jonction neuro-musculaire.
2.2. Les récepteurs de l’acétylcholine
On distingue 2 types de récepteurs : les récepteurs muscariniques divisés en 5 classes de M1 à M5, et les récepteurs nicotiniques neuronaux N1 (système nerveux central et ganglions périphériques et musculaires), et les récepteurs nicotiniques de type musculaires de type N2.
| Tissu | Effet de l’acétylcholine | Récepteurs impliqués |
|---|---|---|
| Système nerveux | Mémorisation et apprentissage | M1 |
| Cœur | Diminution de la fréquence cardiaque | M2 |
| Vaisseaux | Vasodilatation, baisse de la pression artérielle | M3 |
| Poumon | Contraction des bronches, sécrétion | M3 |
| Intestins, estomac | Contractions, sécrétions | M3 |
| Glandes salivaires | Sécrétion | M3 |
| Œil | Contraction de la pupille, larmes | M3 |
| Glande médullosurrénale | Inhibe la sécrétion d’adrénaline (qui n’est plus stimulée par le système orthosympathique) | N |
| Muscle squelettique | Contraction | N |
Action de l’acétylcholine [17] dans le système nerveux périphérique
2.3. Le rôle de l’acétylcholinestérase
Dans tous les cas, l’ACh doit disparaître rapidement de la synapse après sa libération et pour cela, elle est hydrolysée par une enzyme, l’acétylcholinestérase (AChe) en quelques millisecondes en acétate et en choline.
3. Les inhibiteurs des acétylcholinestérases
3.1. En médecine
Dans certaines maladies, il est nécessaire d’accroître la transmission cholinergique, par exemple en apportant des agonistes (non hydrolysables) des récepteurs cholinergiques (muscarine, alcaloïdes, nicotine). On peut aussi utiliser des inhibiteurs de l’acétylcholinestérase comme la physostigmine, la pyridostigmine et divers autres inhibiteurs sont testés pour traiter les déficiences cholinergiques associées à la maladie d’Alzheimer (rivastigmine).
On peut aussi, plus spécifiquement, utiliser des antagonistes des récepteurs de l’ACh comme la belladone et l’atropine.
3.2. Les organophosphorés neurotoxiques
Ces molécules organophosphorées neurotoxiques bloquent l’acétylcholinestérase (AChE). C’est le cas du sarin.
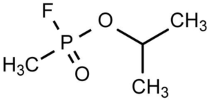
En bloquant l’acétylcholinestérase, l’acétylcholine s’accumule au niveau des synapses et stimule à l’excès les nerfs, les muscles et les glandes (notamment les glandes lacrymales), les glandes salivaires et les glandes sudoripares dans l’ensemble de l’organisme. Au début, les muscles stimulés tremblent puis se contractent de manière incontrôlable, puis dans un deuxième temps ils se fatiguent et s’affaiblissent.
L’exposition à des agents neurotoxiques peut entraîner des troubles neurologiques et neurocomportementaux à long terme, notamment une anxiété, une dépression, une irritabilité et des problèmes de mémoire (MSD [18]).
4. Mode d’action des organophosphorés
Ils se fixent aux cholinestérases quelles qu’elles soient et occupent en le phosphorylant le site estérasique de l’enzyme, s’opposant ainsi à l’hydrolyse physiologique de l’acétylcholine en choline et en acide acétique. La déphosphorylation de l’enzyme inhibée par l’OP est très lente, mais peut être accélérée par un réactivateur des cholinestérases ou « oxime » qui fait partie du traitement actuel de l’intoxication.
À température ambiante le sarin est un liquide qui s’évapore facilement attaquant alors l’individu par voie cutanée et respiratoire. L’exposition de la peau à ces agents cause initialement des contractions et de la transpiration au site de l’exposition. Des effets affectant l’ensemble de l’organisme surviennent après un certain délai pouvant durer jusqu’à 18 heures après l’exposition d’un agent G ou V.
Les agents neurotoxiques stimulent les cellules nerveuses dans le cerveau et les personnes deviennent agitées, confuses, et sujettes à des crises convulsives ou perdent connaissance.
La stimulation des cellules nerveuses en dehors du cerveau provoque la nausée, des vomissements, des larmes, des sécrétions nasales, une salivation importante, des sécrétions pulmonaires, une respiration sifflante, des sécrétions digestives exagérées (telles que diarrhée et vomissements), et de la transpiration. La stimulation des cellules musculaires entraîne des crampes suivies de faiblesse et de paralysie. La faiblesse des muscles respiratoires et l’interruption du centre respiratoire dans le cerveau constituent habituellement la cause du décès.
Le diagnostic sur le terrain est réalisé par un médecin qui s’appuie sur l’histoire du terrain, le toxidrome [19] et l’utilisation de papier détecteur [20], ou d’autres types de détecteurs.
5. Traitement de l’intoxication au sarin
5.1. Traitement symptomatique et anticonvulsivant
Le traitement symptomatique est essentiellement la réanimation respiratoire. Elle repose sur les différentes mesures de libération des voies aériennes et d’oxygénothérapie, qui peuvent aller jusqu’à l’intubation et la ventilation contrôlée du patient. Son efficacité, bien établie, est limitée en cas d’afflux massif.
Le traitement anticonvulsivant indispensable repose sur les benzodiazépines (Valium) et sans doute de façon plus récente sur la kétamine.
Deux médicaments sont généralement administrés : l’atropine et le pralidoxime.
5.2. L’atropine
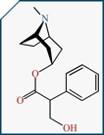
L’atropine est le véritable antidote de l’intoxication aux OP. L’atropine agit en compétition avec l’acétylcholine au niveau des récepteurs muscariniques, mais elle est sans effet sur les cholinestérases de la jonction neuromusculaire. L’atropine bloque les récepteurs de l’ACh empêchant alors cette dernière de continuer à stimuler les neurones.
5.3. La pralidoxime
La pralidoxime est un réactivateur des cholinestérases qui hydrolyse la liaison enzyme-inhibiteur, mais également l’inhibiteur et agit en synergie avec l’atropine permettant la diminution des doses de celle-ci. Elle se fixe sur le groupement alkyl-phosphate de la cholinestérase alkyl-phosphorylée et le détache de l’acétylcholinestérase qui est ainsi régénérée.
Il existe des auto-injecteurs contenant les 2 produits.
Sous la forme déalkylée, l’enzyme n’est plus réactivable.
5.4. La phosphorylation de la cholinestérase
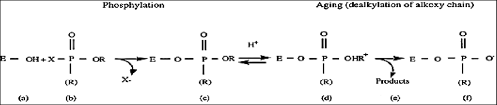
Illustration du mécanisme de phosphorylation et de vieillissement de la cholinestérase. (a) enzyme libre ; ( b) composé organophosphoré ; (c) enzyme phosphorylée ; (d) intermédiaire ; (e) produits de désalkylation et (f) enzyme vieillie.
Sous la forme déalkylée, l’enzyme n’est plus réactivable
5.5. Mode d’action de la pralidoxime : réactivation de la cholinestérase
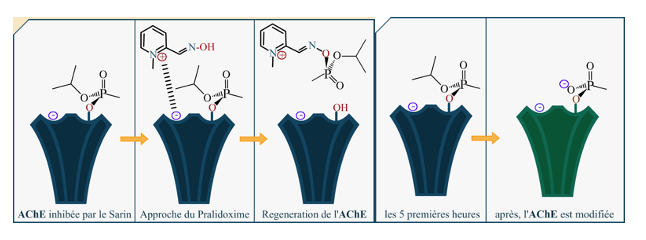
Le mode d’action de la pralidoxime n’est plus valide si l’exposition au sarin dépasse les 5 heures, conséquence d’un processus de vieillissement de l’AChE sur le long terme, également appelé « Aging Process ».
Processus du vieillissement de l’AChE après 5 heures d’exposition au Sarin – AChE détériorée (ici en vert).
Ces figures très pédagogiques sont tirées de l’article consacré au Sarin de la revue « Zeste de savoir [21]»
6. La décontamination
Elle réduit la dose d’organophosphoré absorbée au niveau de la peau et évite un transfert de contamination vers l’entourage (DECPOL ABS [22]). En cas d’alerte chimique, la nature du toxique, souvent inconnue, augmente le nombre de victimes potentielles avec risque majeur de transfert de contamination (voir la situation des soignants lors de l’attaque au gaz sarin dans le métro de Tokyo).
7. Le syndrome de la guerre du Golfe
Dans un article [23] précédent nous avons fait état des nombreux cas d’utilisation du gaz sarin, tant du point de vue terrorisme que du point de vue étatique. Il est conseillé de se le remémorer afin de constater que c’est un produit qui a été largement employé.
Les rapports sur le « syndrome de la guerre du Golfe » ont donné lieu à des spéculations sur les associations possibles entre les expositions toxiques.
L’uranium appauvri n’a pas été retenu comme cause, ce qui laisse l’exposition aux composés organophosphorés en aérosol (pesticides et agent neurotoxique sarin) comme cause(s) plus probable(s) du syndrome de la guerre du Golfe.
Dans une étude intéressante de H. M. Bolt, la question était posée de savoir si le sarin pouvait avoir joué un rôle dans le syndrome de la guerre du Golfe.
L’étude du polymorphisme génétique du génotype Q192R de la paraoxonase-1 (PON1) peut fournir des informations sur son association avec certaines conditions ou maladies, notamment des troubles métaboliques tels que le diabète de type 2, l’obésité, ou d’autres maladies cardiovasculaires.
Dans notre cas, on a cherché à savoir si le syndrome de la guerre du Golfe a une relation avec l’exposition à de faibles doses d’agents neurotoxiques.
L’étude a été menée sur 508 soldats malades comparés à 508 soldats témoins non malades. L’exposition à de faibles doses d’agents neurotoxiques a été estimée à l’aide de questions d’enquête sur le fait d’avoir entendu des alarmes sonores d’agents neurotoxiques sur le terrain.
Les études ont montré que l’interaction gène-environnement du génotype Q192R et des alarmes auditives a été fortement associée à la maladie de la guerre du Golfe.
Au total, ces données soutiennent l’idée d’une relation de cause à effet entre les composés organophosphorés de faible niveau, en particulier le sarin, et les symptômes de la maladie de la guerre du Golfe. Dans la presse non spécialisée, des spéculations ont été avancées sur un lien avec le bombardement de la cache d’armes chimiques de Saddam Hussein en janvier 1991 autour des villes de Muthanna et Fallujah, qui avait libéré du sarin.
Étant donné la complexité des actions toxiques systémiques du sarin, en particulier celles qui affectent le cerveau et l’absence d’antidotes efficaces contre les lésions du système nerveux central, la recherche sur la toxicité du sarin peut se poursuivre encore longtemps.
📚 Bibliographie
- Hermann M. Bolt, Sarin: a never-ending story, Archives of Toxicology, en ligne le 28 novembre 2022
- Intoxications par les organophosphorés, Consensus d’actualisation SFAR – Médecine d’urgence 1999, J. M. Saïssy, M. Rüttimann
- Acétylcholine, Wikipédia, consulté le 3 mars 2024
- UA Okoli, NI Nubila and MT Okafor, Organophosphorous Pesticide: An Environmental Pollutant Perspective, Journal of Chemical and Pharmaceutical Research, 2017, 9(9):126-130
8. Questions fréquentes
Comment le sarin agit-il sur le système nerveux ?
Le sarin bloque l’acétylcholinestérase (AChE), l’enzyme chargée de dégrader l’acétylcholine dans la synapse. En l’absence de cette dégradation, l’acétylcholine s’accumule et stimule en excès les nerfs, les muscles et les glandes. Cette crise cholinergique provoque tremblements, convulsions, paralysie musculaire et, dans les cas graves, l’arrêt respiratoire et la mort.
Pourquoi la pralidoxime doit-elle être administrée rapidement après une intoxication au sarin ?
La pralidoxime réactive l’acétylcholinestérase en détachant le sarin de l’enzyme. Mais au-delà de 5 heures d’exposition, l’enzyme subit un processus de vieillissement irréversible (« Aging Process ») : sous sa forme déalkylée, elle ne peut plus être réactivée. Passé ce délai, la pralidoxime devient inefficace, ce qui rend l’administration précoce absolument critique.
Quelle est la différence entre l’atropine et la pralidoxime dans le traitement ?
L’atropine agit en bloquant les récepteurs muscariniques de l’acétylcholine, empêchant cette dernière de stimuler les neurones, sans toucher aux cholinestérases. La pralidoxime, elle, réactive directement l’acétylcholinestérase inhibée par le sarin. Les deux médicaments agissent en synergie : la pralidoxime permet de réduire les doses d’atropine nécessaires. Des auto-injecteurs contenant les deux produits existent pour une administration rapide sur le terrain.
Le sarin peut-il provoquer des séquelles à long terme ?
Oui. L’exposition à des agents neurotoxiques comme le sarin peut entraîner des troubles neurologiques et neurocomportementaux durables : anxiété, dépression, irritabilité et problèmes de mémoire. Le syndrome de la guerre du Golfe illustre ce risque : des études ont établi un lien probable entre l’exposition à de faibles doses d’organophosphorés, dont le sarin, et les symptômes chroniques développés par des milliers de vétérans.
Pourquoi la décontamination est-elle indispensable lors d’une attaque au sarin ?
Sans décontamination rapide, le sarin continue d’être absorbé par la peau et peut contaminer secondairement le personnel soignant. Lors de l’attentat du métro de Tokyo en 1995, l’absence de mesures de décontamination a exposé près de 20 % du personnel hospitalier à des symptômes (douleurs oculaires, dyspnée, nausées). La décontamination réduit la dose absorbée et protège l’ensemble de la chaîne de secours.