À l’heure ou la pandémie au Covid-19 continue à s’étendre sur notre territoire, nous allons nous intéresser aux différents traitements actuellement testés et potentiellement capables d’enrayer la progression de la maladie chez l’homme.
La maladie
Ce qui surprend avec le Covid-19, c’est l’extrême variabilité de la maladie. Les signes cliniques classiques apparaissent après une période d’incubation de 1 à 14 jours (aux alentours de 5 jours dans la majorité des cas). Il y a de la fièvre vers 38°C, une toux sèche parfois irrépréhensible et une grande fatigue accompagnée de douleurs musculaires. L’essoufflement et les difficultés respiratoires peuvent apparaître vers le 7ème jour de la maladie. Dans certains cas il y a une perte du gout et de l’odorat (anosmie) ce qui est assez caractéristique de la maladie. Chez certains patients, vers le 10ème jour peut se produire une dégradation brutale des fonctions respiratoires menant à une syndrome respiratoire aigu sévère alors que la charge virale semble diminuer : ceci est dû à une réponse inappropriée du système immunitaire au niveau pulmonaire qui sur sur-réagit à la présence du virus.
Un grand nombre d’individus n’expriment aucun symptôme tout en répandant autour d’eux des virus : ce sont des porteurs sains. Des signes cliniques peuvent manquer alors qu’on peut en voir d’autres moins fréquents comme la diarrhée.
Le but d’un traitement est de faire baisser la charge virale dès le début de la maladie avant que les symptômes respiratoires sévères n’apparaissent.
Le virus
Structure
Le coronavirus responsable du Covid-19 est le SARS-CoV-2. C’est un virus dit « enveloppé ». Il est constitué d’une molécules d’ARN simple brin liée à des protéines (= nucléocapside) et d’une enveloppe formée des structures lipidiques membranaires de la cellule dans laquelle il s’est multiplié. De cette structure sortent des « spikes », structures protéiques apparaissant sous la forme d’une couronne, (d’où le nom de coronavirus) et qui vont servir de point d’encrage sur les récepteurs cellulaires. Il mesure entre 100 et 150 nm.
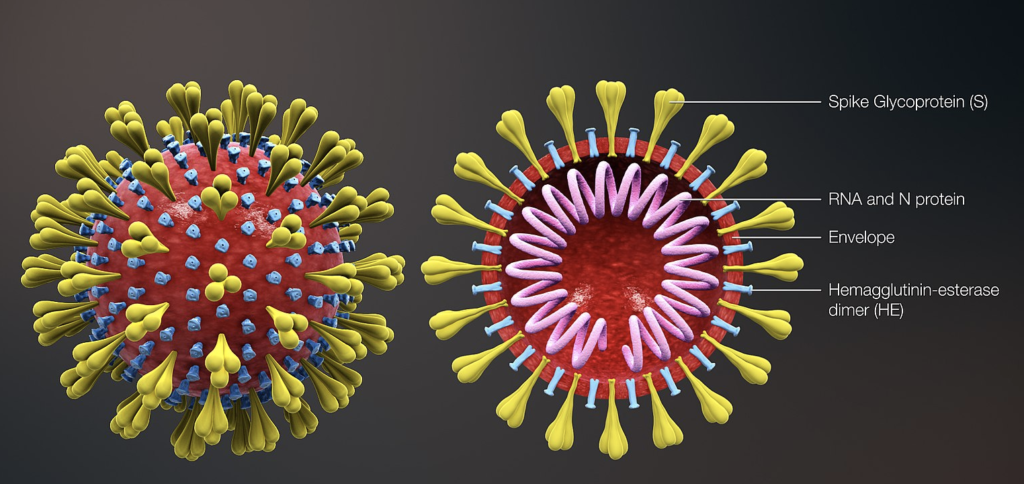
Un virus est incapable de se reproduire seul. Il pénètre dans une cellule vivante pour l’obliger à fabriquer des virus à son image. À la fin du processus, les virus s’échappent de la cellule qui s’épuise. Ils vont alors s’attaquer aux cellules avoisinantes pour se multiplier. La maladie est la conséquence de la destruction des cellules, donc des tissus, parfois aggravée par une réponse inappropriée du système immunitaire qui libère des substances nocives attaquant à leur tour les tissus.
Reproduction
Pour se reproduire dans la cellule cible le virus doit
1- Entrer dans la cellule
2- Libérer son ARN qui servira de matrice pour synthétiser des molécules ARN identiques qui constitueront les nouveaux virus
3- synthétiser les 16 protéines qui seront emmenées dans les particules virales nouvellement synthétisées avec l’ARN.
4- Sortir de la cellule
Les différentes étapes et les stratégies pour inhiber le virus
1- Entrée dans la cellule
a- Entrée par fusion des membranes
Comme dans un système « clé-serrure » le virus va s’attacher à nos cellules par l’intermédiaire de ses « spikes » qu’il va accrocher aux récepteurs de nos cellules appelés ACE2. Avant que la fixation ne se produise il faut que les spikes soient « activés » par une protéase qui les scinde en 2 parties. Cette protéase est elle-même présente sur la membrane de nos cellules et elle s’appelle la TMPRSS2.
L’attachement est suivi de la fusion de la membrane du virus et de la membrane cellulaire ce qui permet à l’ARN de pénétrer à l’intérieur de la cellule.
Pour résumer : Le spike est activé par l’enzyme TMPRSS2 et peut s’attacher au récepteur ACE2.
Stratégies antivirales :
Bloquer les spikes par des anticorps qui se trouvent dans le plasma de personnes guéries du Covid-19 : c’est la « plasmothérapie ».
Bloquer l’activité de l’enzyme chargée d’activer le spike, la TMPRSS2 par un médicament appelé le mésylate de Camostat.

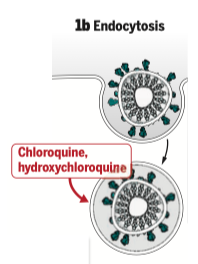
b- Entrée par endocytose
Comme beaucoup de virus enveloppés, le virus peut aussi entrer dans la cellule en étant totalement absorbé dans une vacuole : c’est « l’endocytose ». La vacuole se forme après contact des membranes, consécutif là aussi à l’activation des spikes par la TMPRSS2. Le virus doit alors sortir de la vacuole pour pouvoir se « déshabiller » à l’intérieur de la cellule, c’est à dire se débarrasser de son enveloppe et libérer l’ARN des protéines qui l’entourent. Cette étape nécessite une variation de pH. C’est là qu’intervient la chloroquine (ou l’hydroxychloroquine moins toxique) qui empêche cette variation de pH, enrayant ainsi l’entrée du virus. Son association avec l’azithromycine, un antibiotique utilisé contre les bactéries intracellulaires permettrait une potentialisation de son effet.
2- Synthèse des ARN des futurs virus
L’ARN viral qui a pénétré dans la cellule est copié par une enzyme à l’origine présente dans le virus : l’ARN polymérase.
Un médicament développé contre le virus EBOLA et appelé « Remdesivir » est capable de bloquer la synthèse de ces ARN en induisant des erreurs non réparables par les systèmes de correction qui existent pourtant chez ce virus.
3- Synthèse des protéines qui seront emportées par le virus
Les virus sont constitués d’un génome qui est l’ARN et de 16 protéines qu’il emporte avec lui (dont l’ARN polymérase vue ci-dessus).
N’ayant pas les capacités de synthèse des protéines par lui-même, il va se servir de l’appareil de synthèse de la cellule infectée : les ribosomes.
Le code de synthèse est « l’ARN messager » qui a été synthétisé lui aussi à partir de l’ARN viral.
Les ribosomes de la cellule se déplacent sur l’ARN messager et ajoutent bout à bout les bons acides aminés pour former la protéine.
C’est donc bien la machinerie cellulaire qui synthétise les protéines du virus.
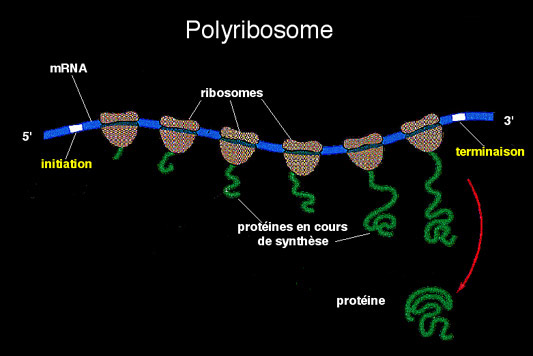
Dans la réalité, c’est une grande protéine qui est synthétisée avant d’être découpée en morceaux qui seront les 16 protéines emportées par le virus. Ce découpage est réalisé par une protéase virale dont un inhibiteur a été mis au point pour lutter contre le virus du sida : il s’agit de l’association « Lopinavir-ritonavir » (Kaletra), le lopinavir inhibe la protéase tandis que le ritonavir protège le lopinavird’une dégradation trop rapide.

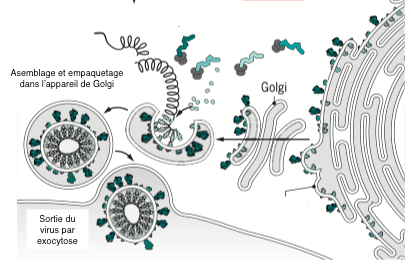
Les différents éléments, ARN et protéines, s’assemblent spontanément dans le cytoplasme de la cellule puis sont empaquetés dans l’appareil de golgi. Les nouveaux virus sont rejetés dans le milieu extérieur en emportant avec eux de la membrane cellulaire. C’est pourquoi on les appelle des virus enveloppés. Aucune de ces étapes n’est la cible d’un traitement antiviral.
Les autres stratégies
Un grand nombre d’autres pistes sont explorées comme :
- Faire agir des anticorps monoclonaux dirigés contre les spikes à la place des anticorps naturels se trouvant dans le plasma de patients guéris ;
- Ajouter au mélange Lopinavir- ritonavir un stimulant de l’immunité comme l’interféron bêta ;
- Booster le système immunitaire en vaccinant le patient malade avec du BCG (Bacille Bilié de Calmette et Guérin) bien connu pour ses propriétés immunostimulantes.
- …
Un essai clinique, baptisé Discovery a démarré le 23 mars en France pour tester 4 traitements expérimentaux. Il est piloté par Florence Ader, infectiologue dans le service des maladies infectieuses et tropicales à l’hôpital de la Croix-Rousse au CHU de Lyon et chercheuse au Centre international de recherche en infectiologie CIRI (Inserm/CNRS /Université Claude Bernard Lyon 1).
L’objectif est d’évaluer l’efficacité et la sécurité de quatre stratégies thérapeutiques expérimentales qui pourraient avoir un effet contre le Covid-19 au regard des données scientifiques actuelles.
L’essai DISCOVERY démarre avec 5 modalités de traitement :
- soins standards ;
- soins standards plus remdesivir ;
- soins standards plus lopinavir et ritonavir ;
- soins standards plus lopinavir, ritonavir et interféron bêta ;
- soins standards plus hydroxy-chloroquine.
Ces travaux incluent 3 200 patients hospitalisés dans toute l’Europe, dont 800 en France. Cet essai clinique est évolutif. Si une des molécules sélectionnées est inefficace, elle est abandonnée. À l’inverse, si l’un d’entre elles marche sur un des patients, elle pourra être testée sur tous les patients dans le cadre de l’essai.
Cet essai complètera l’étude SOLIDARITY lancée avec à peu près les même molécules, depuis le 20 mars par l’OMS sur plusieurs milliers de patients dans différents pays.
On remarquera que les molécules testées sont connues ainsi que leurs effets toxiques ce qui permettra d’aller beaucoup plus vite dans leur mise en œuvre lorsque les résultats seront connus.
Conclusion
Trouver un traitement permettant d’éviter les complications respiratoires entrainant la mort des patients atteints du Covid-19 est une urgence absolue. Il a donc été décidé de tester des molécules déjà sur le marché dont on connaît bien les effets secondaires toxiques. Les résultats de ces tests ne devraient pas tarder maintenant.
D’autres équipes travaillent sur la mise au point d’un vaccin qui protègera les populations lorsque la maladie reviendra. Mise au point difficile et très longue mais néanmoins indispensable pour éviter ce genre de pandémie qui ne s’était pas produite depuis celle de la grippe ne 1918-19.
Auteur : Professeur François Renaud




2 commentaires
Bonjour,
et merci pour cet article très intéressant. Comme beaucoup de Français, je me pose la questions de savoir quand et où je pourrai me procurer les masques réutilisables Michelin FFP2 OCOV.
Peut -on acheter aussi des articles sur votre site ?
Merci de votre réponse….et bon courage dans vos recherches
Cordialement
Merci de votre intérêt pour OCOV. Nous nous concentrons la fabrication, sa qualité et nous appuyons sur un réseau de distributeurs tres professionnels poyr la commercialisation, les plus connus poyr le grand public: FNAC DARTY